Revista
Papel del tejido duro en el mantenimiento del tejido periimplantario
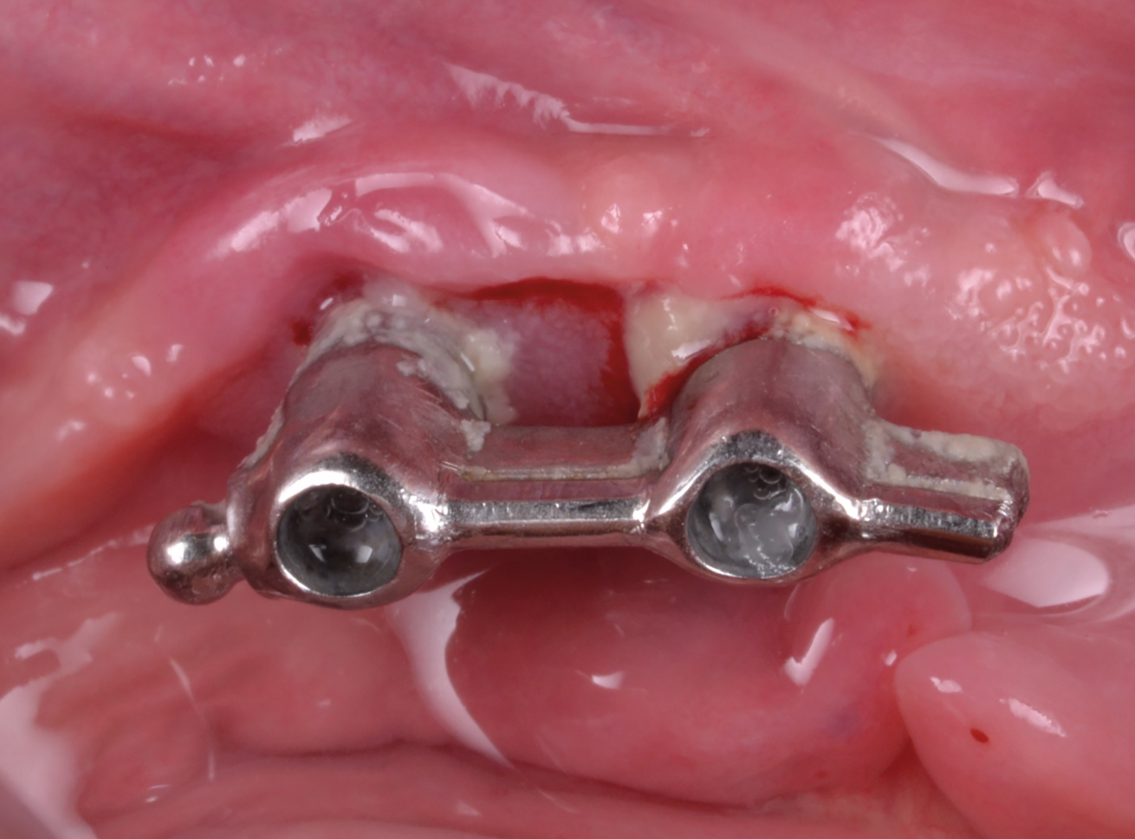 Las patologías periimplantarias representan la mayor amenaza para la supervivencia y éxito de los implantes a largo plazo. Mientras que clásicamente se entendió que la pérdida de hueso periimplantaria era inevitable y que posiblemente pudiera no repercutir negativamente en el éxito a largo plazo, definiciones actuales de periimplantitis hacen referencia a la pérdida de hueso progresiva como indicador de patología. Por ello, el clínico debe entender los principios biológicos de remodelación ósea y cómo poder manejarlos para minimizar la reabsorción de hueso como consecuencia del proceso fisiológico posquirúrgico y de establecimiento y anclaje del tejido conectivo supracrestal alrededor de los implantes.
Las patologías periimplantarias representan la mayor amenaza para la supervivencia y éxito de los implantes a largo plazo. Mientras que clásicamente se entendió que la pérdida de hueso periimplantaria era inevitable y que posiblemente pudiera no repercutir negativamente en el éxito a largo plazo, definiciones actuales de periimplantitis hacen referencia a la pérdida de hueso progresiva como indicador de patología. Por ello, el clínico debe entender los principios biológicos de remodelación ósea y cómo poder manejarlos para minimizar la reabsorción de hueso como consecuencia del proceso fisiológico posquirúrgico y de establecimiento y anclaje del tejido conectivo supracrestal alrededor de los implantes.
Autores: Dres. Alberto Monje, Francesco di Leone, Blanca Paniagua, Andrés Pascual y José Nart.
Introducción
Los primeros pasos dados en la implantología oral contemporánea concebían el éxito simplemente en la incorporación de un material aloplástico, es decir, de un material inerte, en hueso vital a través de la reparación originada tras el trauma quirúrgico. Los estudios en animales llevados a cabo por el Prof. Brånemark desde 1952, primero en el Laboratorio de Microscopía de la Universidad de Lund y posteriormente en el Laboratorio de Biología Experimental de la Universidad de Gotemburgo, asentaron las bases biológicas y el fundamento en implantología. En virtud de todos los hallazgos preclínicos se definió “osteointegración” como el íntimo contacto a nivel microscópico entre un implante y el hueso (Brånemark y Albrektsson 1982).
En base a ese fundamento biológico revolucionario se constituyeron años más tarde criterios de “éxito” que concebían de nuevo el hueso como el parámetro crucial. En este sentido resulta interesante destacar que dichos criterios aceptaban una estabilidad relativa del nivel óseo determinado radiográficamente. Por ejemplo, inicialmente Albrektsson y cols. definieron “éxito” dentro de un contexto flexible aceptando una pérdida ósea de 1,5 mm como resultado de una pérdida inicial o fisiológica y de una pérdida de hueso anual de 0,2 mm. Otros criterios de “éxito” publicados subsecuentemente tendían a centrarse más, aunque de un modo muy ambiguo y subjetivo, en la ausencia de patologías y la satisfacción del paciente (Misch y cols. 2008; Papaspyridakos y cols. 2012).
Por otro lado, y de un modo muy acertado, el campo de la periodoncia se ha centrado las últimas dos décadas en el estudio de la estabilidad ósea como criterio para determinar el pronóstico de los implantes dentales en virtud de la presencia/ausencia de patología (Lindhe y cols. 2008; Sanz y cols. 2012). En otras palabras, la preocupación evidente no es el hecho de que pueda haber o no “éxito”, sino la presencia de patología o de salud.
1. Estado actual del nivel óseo como indicador de estabilidad
La estabilidad del nivel óseo se ha considerado clásicamente como un indicador de salud periimplantaria. Cierto es que puede haber presencia de patología confinada en los tejidos blandos en ausencia de pérdida de hueso (mucositis periimplantaria). Sin embargo, al contrario que la periimplantitis, la mucositis es una patología reversible de modo predecible y cuya evolución aún se desconoce por completo si siempre desemboca en periimplantitis (Heitz-Mayfield y Salvi 2018).
La definición actual de periimplantitis elaborada por el consenso mundial sobre la clasificación de las enfermedades periodontales y periimplantarias indica que para poder aseverar la ocurrencia de pérdida ósea como respuesta a un proceso patológico debe tratarse de pérdida ósea progresiva observada entre dos puntos en el tiempo (Berglundh y cols. 2018; Schwarz y cols. 2018).
Para poder diagnosticar de un modo certero dicha progresión en la pérdida de hueso, y evitar un diagnóstico incorrecto, se deben tener en cuenta los siguientes elementos (Renvert y cols. 2018):
- Para poder identificar la pérdida de hueso progresiva es conveniente evaluar el nivel óseo en radiografías estandarizadas. De lo contrario, se recomienda un error estándar asumible de 0,5 mm debido a inexactitudes inherentes a la técnica radiográfica.
- Para poder cerciorarse de que la remodelación ha ocurrido como consecuencia de un proceso patológico, se recomienda realizar una radiografía (preferiblemente intraoral siguiendo la técnica de paralelismo) en el momento de la carga definitiva de la prótesis, y 12 meses después.
- Si durante los primeros 12 meses ocurre una pérdida ósea ≥2 mm con respecto a los niveles óseos en el momento de la carga de la prótesis, se considera pérdida patológica.
De carecer de una radiografía tras el proceso inicial de remodelado fisiológico, un umbral de pérdida ósea >3 mm en presencia de parámetros clínicos inflamatorios es compatible con la definición de caso de periimplantitis (Renvert y cols. 2018) (Figura 1).
2. Estabilidad ósea como factor pronóstico
Como se ha contextualizado previamente, en la breve historia de la implantología moderna, la heterogeneidad en términos de “éxito” y de definición de patología periimplantaria han dificultado alcanzar un consenso global para poder pronosticar de un modo certero implantes que presentan pérdida de hueso. Un aspecto que sí está claro es que, con la incorporación de las superficies microrugosas en los implantes con el fundamento de mejorar la esencia de la osteointegración, en el momento en el que hay exposición de la superficie al surco periimplantario, el resultado es la contaminación por bacterias patógenas. Esta infección desencadena una serie de eventos biológicos que se encargan de perpetuar una patología crónica que, en caso de no ser resuelta, conduce a la pérdida progresiva de hueso. Estudios en humanos han demostrado que la pérdida de hueso alrededor de implantes ocurre siguiendo patrones no lineales (Papantonopoulos y cols. 2015; Derks y cols. 2016) (Figura 2).
Por lo tanto, el principal objetivo para minimizar el riesgo de infección es anticipar que el implante, durante su colocación y posterior remodelación ósea como resultado del trauma quirúrgico, quede completamente embebido en hueso (Figura 3).
3. Pérdida de hueso periimplantario como resultado de la remodelación fisiológica
La exposición de los implantes al medio oral tras el proceso de osteointegración y durante el primer año de carga va acompañada de un remodelado óseo fisiológico a nivel crestal y de tejidos blandos, resultado de la instauración del clásicamente denominado “espacio biológico”. Este se establece como resultado de las cuatro fases de cicatrización tras la conexión del componente transmucoso: hemostasia, fase inflamatoria, fase proliferativa y fase de remodelado y siguiendo los principios de cicatrización por segunda intención, la cual se caracteriza por la capacidad contráctil de los miofibroblastos (Tatarakis y cols. 2012; Hsu y cols. 2016).
3.1. Hallazgos clínicos y preclínicos
De un modo genérico, en implantes de una pieza, esta pérdida ósea temprana oscila entre 0,2-0,7 mm (Hermann y cols. 2000a; Hermann y cols. 2000b), y en implantes de dos piezas entre 1-1,5 mm durante el primer año en función, seguida de una pérdida ósea anual de 0,1-1,5 mm (Malmqvist y Sennerby 1990; Cochran y cols. 1997; Hermann y cols. 1997; Bravi y cols. 2007; Galindo-Moreno y cols. 2015). Sin embargo, los niveles óseos marginales actuales alrededor de implantes después de la carga protésica se mantienen estables, no superando los 0,5 mm de pérdida ósea a los 3 y 5 años de seguimiento (Laurell y Lundgren 2011).
En la Tabla 1 se resumen todos aquellos factores asociados a pérdida ósea que han sido demostrados por la evidencia científica.
3.2. Justificación biológica
La mucosa periimplantaria consta de un epitelio de unión de 1,5-2,0 mm y una zona de tejido conectivo de 1,0-1,5 mm, formando una inserción de tejido blando supracrestal de 3,0-4,0 mm (Berglundh y cols. 1991). Asimismo, otros estudios han observado que el remodelado óseo se produce, no solo por la formación de un sellado biológico, sino también por la colonización bacteriana en la unión implante-pilar, debido a la presencia de un microespacio o microgap y de los micromovimientos producidos en esta interfase (Mombelli y cols. 1987; Ericsson y cols. 1995), por el trauma quirúrgico, la posición del implante en relación a la cresta ósea, las características de superficie y el diseño de los implantes en la región cervical, el tipo de conexión entre implante y pilar, la distancia interimplantaria, la manipulación del pilar, la sobrecarga oclusal y la periimplantitis (Oh y cols. 2002). Otro aspecto importante a considerar en el establecimiento del espacio biológico y, por consiguiente, en el remodelado óseo inicial, es el grosor de la mucosa periimplantaria, ya que si este es menor a 2 mm, se producirá una mayor pérdida ósea (Linkevicius y cols. 2009a). De tal modo que en aquellas situaciones en las que no existe suficiente espacio para el establecimiento del espacio biológico se producirá reabsorción ósea para favorecer su estabilización.
4. Marco vestíbulo-lingual: definiendo la distancia vestibular crítica
Varios estudios han evidenciado la importancia del ancho de la cresta alveolar, en particular en lo que respecta al grosor de la pared de hueso vestibular, en la tasa de supervivencia de los implantes. Resulta interesante que en una gran parte de las periimplantitis diagnosticadas, independientemente de la configuración del defecto periimplantario, el denominador común es la pérdida de la pared bucal (Monje y cols. 2019b) (Figura 4). De ahí la importancia de la dimensión de la cresta alveolar en sentido vestíbulo-lingual (Figura 5).
4.1. Hallazgos clínicos y preclínicos
4.1.1. Implantes en alveolos cicatrizados
(implantes diferidos)
Spray y cols. demostraron un aumento en la tasa de fallo temprano en escenarios con <2 mm de tabla ósea bucal, así como mayor inestabilidad de la misma cuando esta era <1,8 mm tras la colocación de implantes (Spray y cols. 2000). Del mismo modo, Barone y cols. reportaron una estabilidad periimplantaria más favorable del tejido duro y blando en presencia de ≥1 mm de pared ósea vestibular (Barone, Alfonsi, Derchi y cols. 2016). Otro estudio mostró de manera similar que la magnitud de la reabsorción ósea vestibular después de la colocación del implante es de aproximadamente 3 mm (Covani y cols. 2004). Esto fue respaldado por otros artículos de recomendaciones clínicas para minimizar las complicaciones estéticas y biológicas (Buser y cols. 2004; Grunder y cols. 2005).
Recientemente, Monje y cols., en un estudio en perros, demostraron que un grosor crítico de la pared de hueso vestibular ≥1,5 mm en la colocación del implante es imprescindible para minimizar la reabsorción fisiológica del hueso. De hecho, se demostró que, en aquellos escenarios por debajo del grosor crítico de hueso bucal, se observaron aproximadamente 4 mm de reabsorción ósea vertical durante las primeras 8 semanas de cicatrización. Además, en un modelo de periimplantitis inducida por ligadura, los mismos autores demostraron que la pérdida ósea como consecuencia de la infección progresa de manera más agresiva en implantes con <1,5 mm de hueso en la cara vestibular. Esto fue consistente con los parámetros clínicos, ya que exhibieron una mayor profundidad de sondaje, más sangrado al sondaje, supuración y recesión de la mucosa en implantes por debajo del grosor crítico del hueso vestibular durante todo el periodo de estudio (Monje y cols. 2019a) (Tabla 2) (Figura 6).
4.1.2. Implantes en alveolos posextracción
(implantes inmediatos)
Desde la publicación de los primeros estudios sobre implantes inmediatos, la creciente cantidad de literatura disponible sobre el tema y la mejoría en los protocolos clínicos han permitido que, en la actualidad y bajo algunas indicaciones, los implantes inmediatos sean considerados una alternativa igualmente predecible a los implantes tempranos o diferidos.
Revisiones sistemáticas recientes demuestran que los implantes colocados en alveolos posextracción presentan tasas de supervivencia comparables a los implantes diferidos. Por ejemplo, Lang y cols. demostraron un 98,4% de tasas de supervivencia para implantes inmediatos tras un periodo medio de 2 años en función (Lang y cols. 2012).
En cuanto a la aparición de complicaciones biológicas, no se han detectado diferencias significativas en la prevalencia de periimplantitis en implantes inmediatos respecto a implantes diferidos durante un periodo de seguimiento de cinco años (Rodrigo y cols. 2012; Jung y cols. 2012). Estudios preclínicos y clínicos han demostrado que el mayor cambio dimensional se observa a nivel vestíbulo-lingual y suele estar provocado por la pérdida del hueso fasciculado, también denominado bundle bone (Schropp y cols. 2003; Araújo y cols. 2005; Araújo y cols. 2006) (Figura 6).
Aunque la colocación de implantes inmediatos se propuso inicialmente con el objetivo de limitar la reabsorción de la tabla vestibular, estudios clínicos y preclínicos han invalidado esta hipótesis ya que, independientemente de la colocación inmediata en alveolos posextracción, la reabsorción ósea y el colapso parcial de los tejidos blandos resulta un proceso inevitable (Blanco y cols. 2008; Tomasi, Sanz, Cecchinato y cols. 2010; Caneva y cols. 2010). No obstante, aunque no se conozcan con certeza, existen una serie de factores relacionados con la anatomía del alveolo y con el procedimiento quirúrgico que parecen influir en la cantidad de reabsorción vestíbulo-lingual tras la colocación de implantes inmediatos (Tabla 3) (Figura 7).
4.2 Justificación biológica
El hueso alveolar está dominado por hueso cortical en la parte más superficial, mientras que la porción central se caracteriza por una estructura más esponjosa. El hueso cortical recibe un aporte sanguíneo desde el exterior a través de los vasos sanguíneos del periostio y desde el interior desde el endostio. Cuando se prepara el lecho para colocar un implante con un procedimiento de colgajo, se interrumpe el suministro de sangre de ambas fuentes. El mismo proceso ocurre desde el interior, ya que la inserción del implante interrumpe el suministro de sangre endostio. Este fenómeno se llama “necrosis avascular” y puede representar un factor crítico en la integridad del hueso periimplantario.
Para implantes inmediatos, sin embargo, la justificación biológica de estos cambios dimensionales se ve alterada por la reabsorción del hueso alveolar propiamente dicho o bundle bone. Este es el hueso cortical avascular que se somete a reabsorción tras la extracción de la pieza dentaria. Sumado a esto, el trauma generado durante la extracción quirúrgica puede también influir en los cambios dimensionales tras la implantación inmediata.
5. Estrategias para minimizar la reabsorción ósea durante la cicatrización temprana
5.1. Regeneración ósea simultánea
En aquellos escenarios con una tabla vestibular fina (<1,5 mm) se recomienda realizar regeneración ósea con el propósito de atenuar los cambios dimensionales que puedan comprometer la integridad del hueso alrededor de implantes dentales tras la remodelación fisiológica. Ante esto, una gran variedad de artículos científicos han sido publicados demostrando la plausibilidad y efectividad de varias técnicas, así como materiales de regeneración para aumento horizontal simultáneo a la colocación de implantes (Sanz-Sánchez y cols. 2015; Benic, Thoma, Jung y cols. 2017; Urban y Monje 2019; Di Raimondo, Sanz-Esporrin, Pla y cols. 2019). A pesar de la ausencia de consenso, la técnica de “aumento de contorno” utilizando hueso autólogo particulado + hueso inorgánico bovino + membrana reabsorbible de colágeno ha sido validada por varios estudios a largo plazo (Buser y cols. 2013a; Buser y cols. 2013b; Chappuis y cols. 2018) (Figura 8).
5.2. Implantes de diámetro estrecho
La atrofia del hueso alveolar representa una limitación para la colocación de implantes dentales en la posición protéticamente guiada. En la mayoría de los casos se propone realizar un procedimiento quirúrgico de reconstrucción y regeneración para aumentar la disponibilidad ósea, con el consecuente inconveniente que estos procedimientos representan al estar asociados a un mayor tiempo, morbilidad y coste para los pacientes, además de un mayor riesgo de complicaciones. Entre las alternativas propuestas está el uso de implantes de diámetro estrecho, considerándose en líneas generales diámetros ≤3,5 mm (Klein y cols. 2014).
En una reciente revisión sistemática (Schiegnitz y Al-Nawas 2018) se comparó la supervivencia de implantes estrechos (clasificados de acuerdo a su diámetro: categoría 1: <3 mm; categoría 2: 3-3,25 mm; categoría 3: 3,25-3,5 mm) con implantes de diámetro regular, así como la pérdida ósea marginal y la calidad de vida de los pacientes. Los resultados para la categoría 1 demostraron una tasa de supervivencia del 94,7%, una media de pérdida ósea marginal en un rango de 0,6-1,43 mm, y un incremento cualitativo en la calidad de vida de los pacientes. En la categoría 2, la media de supervivencia fue de 97,3% sin observarse diferencia con los implantes de diámetro regular, con una media de pérdida ósea marginal entre 0,09-1,6 mm, y sin reportar información sobre cambios en la calidad de vida de los pacientes. Por último, para la categoría 3 se reportó una media de supervivencia de 97,7% sin diferencias con los implantes de diámetro regular, y con una media de pérdida ósea marginal entre 0,1-2,17 mm (Schiegnitz y Al-Nawas 2018).
Estos datos validan, por lo tanto, el uso de los implantes de diámetro estrecho como una alternativa a la regeneración ósea horizontal y con el objetivo de evitar la invasión de la distancia vestibular crítica (Figura 9).
5.3. Minimización del trauma durante el fresado y la colocación de implantes dentales
La creación de un correcto lecho periimplantario es crucial para conseguir estabilidad primaria. Sin embargo, durante el fresado podríamos llegar a generar un trauma por sobrecalentamiento o por el uso de un torque de inserción elevado (necrosis por compresión) y, por ende, una respuesta inflamatoria exacerbada que se traduciría en una futura pérdida ósea periimplantaria, comprometiendo el pronóstico del implante. Tanto con el sobrecalentamiento como con la inserción del implante a un torque demasiado elevado se puede producir una necrosis avascular. Cuando hablamos del torque de inserción sabemos que es importante manejarse entre 24-45 Ncm, ya que si se exceden estos valores se generarán microfracturas y necrosis ósea (Cha, Pereira, Smith y cols. 2015). En un estudio experimental se observó que aquellos implantes colocados a >50 Ncm estaban sujetos a mayor pérdida ósea periimplantaria durante las fases iniciales de curación comparados con aquellos implantes colocados de una forma más pasiva (Duyck, Corpas, Vermeiren y cols. 2010). En relación a las características intrínsecas del hueso, tenemos que tener en cuenta que si la zona que va a albergar un implante tiene un elevado componente de hueso cortical, la cantidad de células osteoprogenitoras será menor que las presentes en un hueso trabecular, y al tratarse de la zona que sufre más tensión, deberíamos extremar las precauciones a la hora de establecer el protocolo de fresado y colocación del implante (Simons y cols. 2015). Por lo tanto, conseguir estabilidad primaria es crucial para la supervivencia del implante; sin embargo, no debemos olvidar que existen una serie de factores, anteriormente mencionados, que tienen lugar incluso antes de que el implante esté integrado y que pueden tener un gran impacto en la preservación del hueso periimplantario.
Conclusiones
Mantener la integridad del hueso alrededor de los implantes tras el proceso fisiológico de remodelado debido al trauma quirúrgico es fundamental para reducir complicaciones biológicas a largo plazo. Para ello es importante conocer todos aquellos factores anatómicos relacionados con el trauma quirúrgico y con el diseño del implante, así como con el componente protético, y ajustarlos con el propósito de minimizar los cambios dimensionales de los tejidos duros y blandos.
Descargar artículo completo
También puede consultar el número 66 de DM El Dentista Moderno

Los representantes del colectivo HIDES Asturias han manifestado su profundo malestar ante una propuesta empresarial que "no solo no mejora las condiciones laborales actuales, sino que incluso plantea retrocesos en derechos básicos".

Gracias al acuerdo de colaboración entre DM-DENTISTA MODERNO y SEPES Bilbao 2025, te ofrecemos 50€ de descuento en tu inscripción al congreso completo. Para ello, introduce el código de descuento BONO-50€ e introduce tus datos para completar el registro. ¡Nos vemos en SEPES Bilbao 2025!

El Consejo General de Dentistas y la Fundación Dental Española han lanzado una campaña para concienciar a los ciudadanos de la importancia de cuidar la salud oral durante las vacaciones.

El Dr. Alberto Monje, Co-Director Médico en Clínica CICOM Monje, nos detalla algúnos de los beneficios que ofrece la implementacion del flujo digital, destacando la mejora en la comunicación con el laboratorio, así como en la precisioin y exactitud de los trabajos.

El uso de alineadores invisibles ha sido ampliamente tratado en la literatura de ortodoncia; sin embargo, aún faltan revisiones sistemáticas y meta-análisis que incluyan una gama amplia de estudios de esta área de la investigación en ortodoncia. El objetivo de la presente contribución es explorar y evaluar la literatura sobre estudios de alineadores invisibles, realizados en edades tempranas de los pacientes. Nuestros resultados sugieren que los artículos disponibles a la fecha presentan en general evidencia científica moderada, independientemente del diseño del experimento. Además, en nuestro análisis exploratorio se detectó algún grado de dependencia respecto de las variables reportadas (i.e., medidas cefalométricas), cuando se testea la heterogeneidad entre estudios. Por último, independientemente de la amplia gama de condiciones diferentes incluidas en los estudios analizados, la mayoría de ellos coinciden en que el tratamiento con alineadores invisibles puede abordar eficientemente la mayoría de las maloclusiones en niños y adolescentes.

En el acto institucional “Donde nacen las ideas: historias reales desde el ecosistema de incubación empresarial”, celebrado en la sede de INCYDE, se ha visibilizado el impacto real y tangible de un modelo pionero de innovación y cohesión territorial.

La Complutense sigue siendo la Universidad más solicitada de la Comunidad de Madrid para el curso 2025-26.

Con el objetivo puesto en simplificar la labor del clínico, el Congreso SEPA Barcelona 2025, que se celebrará del 26 al 29 de noviembre, ha diseñado para esta edición especial un programa práctico y con las últimas tendencias, gracias a la participación de expertos de reconocido prestigio mundial. Así lo avanza en esta entrevista el Dr. Alberto Monje, vocal de la Junta Directiva de SEPA, quien destaca además la perspectiva multidisciplinar de este encuentro en el que tanto la utilidad de las tecnologías emergentes, el uso de inteligencia artificial y el tratamiento de las enfermedades periimplantarias serán protagonistas.

Fumar o vapear no solo afecta a los pulmones, sino que también dificulta la cicatrización, reduce el oxígeno, altera el microbioma bucal y aumenta el riesgo de infecciones como la periimplantitis: una inflamación crónica que puede hacer fracasar el implante incluso años después.

